新(xīn)聞中(zhōng)心
來源:以下文(wén)章來源于Cytiva思拓凡 ,作(zuò)者Li Yafei
2023年2月25日,中(zhōng)華中(zhōng)醫(yī)藥學(xué)會發布了2022年中(zhōng)醫(yī)藥十大學(xué)術進展。張伯禮院士指出:2022年度中(zhōng)醫(yī)藥十大學(xué)術進展主要呈現的價值,就包括“重視新(xīn)技(jì )術新(xīn)方法在中(zhōng)醫(yī)藥中(zhōng)的應用(yòng)”。北京大學(xué)醫(yī)學(xué)部曾克武教授和屠鵬飛教授與浙江大學(xué)、大連醫(yī)科(kē)大學(xué)、博奧生物(wù)研究團隊憑借“新(xīn)技(jì )術助力中(zhōng)藥功效科(kē)學(xué)内涵闡釋”共同獲選2022年度中(zhōng)醫(yī)藥十大學(xué)術進展。
中(zhōng)醫(yī)藥研究者中(zhōng)有(yǒu)廣泛的Biacore用(yòng)戶基礎,曾克武教授和屠鵬飛教授團隊的這一成果裏自然也有(yǒu)Biacore的身影。接下來就讓小(xiǎo)編帶您領略Biacore這一現代科(kē)技(jì ),如何與傳統中(zhōng)醫(yī)藥碰撞并融合,從而闡釋中(zhōng)藥功效科(kē)學(xué)的内涵。
天然産(chǎn)物(wù)中(zhōng)抗腫瘤活性分(fēn)子
發現及作(zuò)用(yòng)機制揭示1
腫瘤免疫微環境(Tumor immune microenvironment ,TIME)調控因子IGF2BP1是一種關鍵N6 -甲基腺苷 (m6A) 閱讀蛋白,識别m6A靶點轉錄物(wù),被認為(wèi)是腫瘤治療的潛在靶點。2022年曾克武教授和屠鵬飛教授團隊發表的研究成果中(zhōng),發現了天然産(chǎn)物(wù)葫蘆素B通過結合IGF2BP1發揮抗腫瘤作(zuò)用(yòng),并且闡釋了作(zuò)用(yòng)機制。
以IGF2BP1為(wèi)出發點,作(zuò)者首先發現,在小(xiǎo)鼠H22荷瘤模型中(zhōng)敲低IGF2BP1,可(kě)以通過免疫細胞招募和降低TIME中(zhōng)PD-L1的表達來抑制肝細胞癌的進展。使用(yòng)Biacore 8K,作(zuò)者驗證了IGF2BP1與甲基化單鏈RNA(ss-m6A)的強親和力,達到了18.3 nM。并且發現,IGF2BP1與非甲基化RNA(ss-A)的親和力則低了13倍。
确定了治療靶點之後,作(zuò)者使用(yòng)Biacore 8K,直接從包含889種化合物(wù)的中(zhōng)藥天然産(chǎn)物(wù)庫中(zhōng)篩選能(néng)抑制IGF2BP1與其m6A靶點的活性分(fēn)子。通過合成生物(wù)素标記的ss-m6A,作(zuò)者将RNA直接固定在芯片上,将化合物(wù)固定濃度(20 μM)與IGF2BP1預孵育,檢測RNA與化合物(wù)- IGF2BP1的結合信号,從而直接篩選出具(jù)有(yǒu)抑制效果的天然産(chǎn)物(wù)(圖1)。
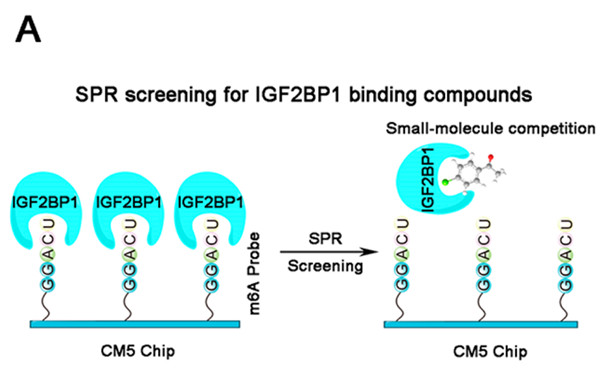
圖1:Biacore 8K抑制劑篩選方法示意圖
通過Biacore 8K的高通量抑制劑篩選實驗,作(zuò)者得到了抑制劑篩選的排序。從圖2中(zhōng)可(kě)以直觀看出,六種具(jù)有(yǒu)較強抑制效果的天然産(chǎn)物(wù)被發現,其中(zhōng)抑制效果最強的當屬葫蘆素B(CuB)。在Huh增殖抑制實驗中(zhōng),葫蘆素B同樣表現出了抑制作(zuò)用(yòng),72h時的IC50達到1.0 uM。
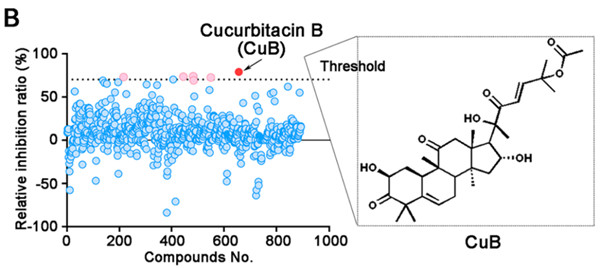
圖2:Biacore 8K抑制劑篩選結果
高通量篩選+精(jīng)确表征,在藥物(wù)研究的各個階段都少不了Biacore。在篩選得到葫蘆素B後,作(zuò)者當然同樣使用(yòng)Biacore精(jīng)确表征了IGF2BP1與葫蘆素B的親和力。結果發現,二者的親和力達到了1.2 μM,與細胞實驗相互印證(圖3)。
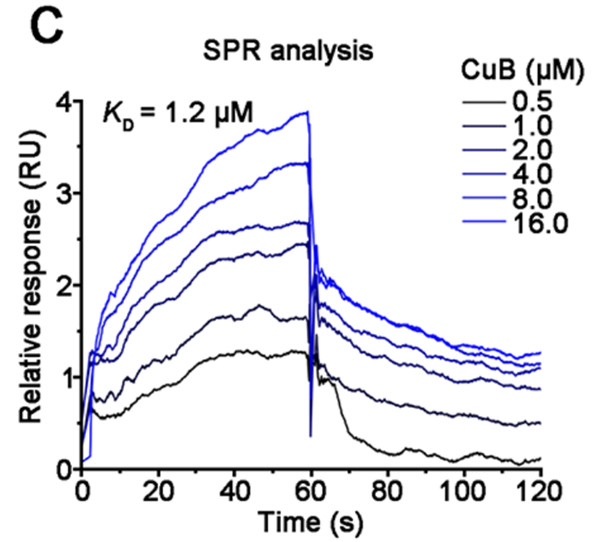
圖3:Biacore精(jīng)确表征IGF2BP1與CuB的親和力
葫蘆素B又(yòu)是什麽呢(ne)?
葫蘆素B是從葫蘆科(kē)等植物(wù)中(zhōng)分(fēn)離得到的一類四環三萜類化合物(wù),具(jù)有(yǒu)廣泛的藥理(lǐ)活性。以葫蘆素B為(wèi)主要成分(fēn)的葫蘆素制劑在臨床治療濕熱毒盛所緻的遷延性肝炎、肝硬化和原發性肝癌具(jù)有(yǒu)确切療效。中(zhōng)藥研究,除了根據已知靶點從天然産(chǎn)物(wù)庫中(zhōng)找活性分(fēn)子外,另一個角度則是已知活性分(fēn)子,尋找作(zuò)用(yòng)靶點。在通過抑制劑篩選及表征,從靶點IGF2BP1出發找到活性分(fēn)子葫蘆素B後,作(zuò)者使用(yòng)“鈎釣”的方法,驗證是否能(néng)利用(yòng)葫蘆素B“鈎”出靶點IGF2BP1。
作(zuò)者首先合成了葫蘆素B分(fēn)子探針,然後利用(yòng)pull-down + 質(zhì)譜的方法從Huh細胞裂解液中(zhōng)成功“鈎”到了靶點IGF2BP1,并且在免疫熒光共定位實驗中(zhōng)證明了細胞中(zhōng)葫蘆素B與IGF2BP1的結合。至此,不論是從靶點出發找活性分(fēn)子,還是從活性分(fēn)子出發找靶點,雙管齊下,作(zuò)者明确了葫蘆素B與腫瘤免疫微環境調控因子IGF2BP1的直接結合。
為(wèi)了進一步闡釋葫蘆素B的抗腫瘤機制,作(zuò)者研究了IGF2BP1上葫蘆素B的結合位置及結合方式。将IGF2BP1的結構域逐一删除後,作(zuò)者發現隻有(yǒu)缺失了C端KH結構域會使IGF2BP1與葫蘆素B不能(néng)結合。通過質(zhì)譜、pull-down、BLAST、CD等多(duō)種方法,作(zuò)者最終确定,葫蘆素B通過邁克爾加成反應結合在IGF2BP1中(zhōng)KH1−2結構域的Cys253上,并且會引起IGF2BP1的構象變化。
那麽葫蘆素B又(yòu)是如何影響IGF2BP1的功能(néng)呢(ne)?
IGF2BP1本身會與ss-m6A結合,前面作(zuò)者使用(yòng)Biacore做了二者抑制劑的高通量篩選,得到了葫蘆素B。高通量抑制劑篩選能(néng)做,單獨的抑制劑表征當然手到擒來。作(zuò)者設置了Biacore實驗來從生化角度上表征葫蘆素B的抑制效果。從結果可(kě)以看出,随着葫蘆素B的濃度逐漸提高,IGF2BP1與ss-m6A的結合信号越來越低(圖4)。Biacore結果與RNA pull-down實驗一緻,明确了葫蘆素B可(kě)以抑制二者結合。
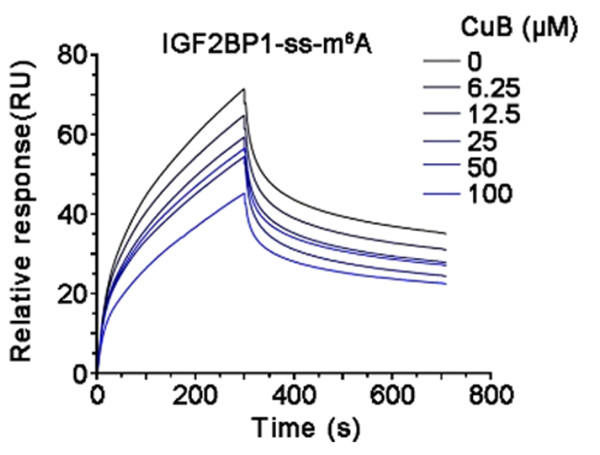
圖4:Biacore實驗明确葫蘆素B抑制IGF2BP1與ss m6A的結合
後續作(zuò)者還發現,葫蘆素B可(kě)以降低與IGF2BP1所結合的mRNA(包括c-MYC、KRAS 等mRNAs)穩定性,在體(tǐ)内通過誘導細胞凋亡,招募免疫細胞到腫瘤微環境,阻斷PD-L1的表達,最終表現出明顯的抗腫瘤效果(圖5)。
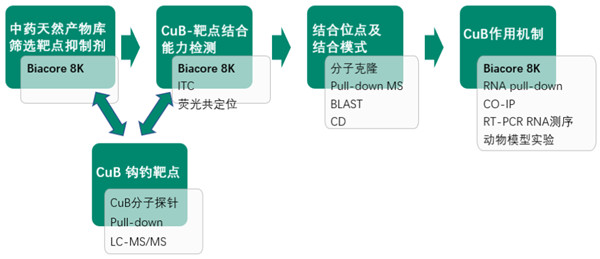
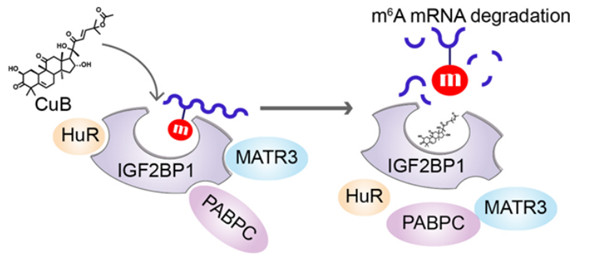
圖5:文(wén)章主要研究路線(xiàn)及作(zuò)用(yòng)機制概述
曾克武教授和屠鵬飛教授團隊專注于天然活性分(fēn)子治療各類型重大疾病的發現及機制闡釋,開發了包括分(fēn)子探針、蛋白芯片2在内的多(duō)種靶點“鈎釣”技(jì )術,多(duō)年以來,許多(duō)研究成果中(zhōng)均使用(yòng)了Biacore作(zuò)為(wèi)生物(wù)分(fēn)子相互作(zuò)用(yòng)檢測技(jì )術。中(zhōng)國(guó)科(kē)學(xué)院院士陳凱先教授指出:年度的學(xué)術進展是中(zhōng)醫(yī)藥學(xué)術研究的“指南針”和“風向标”。相信此次研究成果的入選,也将為(wèi)廣大中(zhōng)醫(yī)藥研究者提供更多(duō)研究思路,對“積極推進中(zhōng)醫(yī)藥科(kē)研和創新(xīn),推動傳統中(zhōng)醫(yī)藥和現代科(kē)學(xué)結合”有(yǒu)重要意義。
Biacore
作(zuò)為(wèi)現代化的體(tǐ)外分(fēn)子互作(zuò)“金标準”,以其超高的靈敏度,超高的數據質(zhì)量,無分(fēn)子量檢測下限,适用(yòng)于各類型的天然産(chǎn)物(wù)及生物(wù)分(fēn)子研究,在中(zhōng)醫(yī)藥研究者中(zhōng)有(yǒu)廣泛的用(yòng)戶基礎。Biacore将持續與廣大中(zhōng)醫(yī)藥研究者勠力同心,共同推動中(zhōng)醫(yī)藥的現代化研究和應用(yòng)。
Biacore,for a better life
參考文(wén)獻:
[1] Liu Y , Guo Q , Yang H , et al. Allosteric Regulation of IGF2BP1 as a Novel Strategy for the Activation of Tumor Immune Microenvironment[J]. 2022.
[2] Zhang et al. Neuroinflammation inhibition by small-molecule targeting USP7 noncatalytic domain for neurodegenerative disease therapy, Sci. Adv. 8, eabo0789 (2022)
