新(xīn)聞中(zhōng)心
為(wèi)何要檢測内毒素 圖片
為(wèi)内毒素無處不在
内毒素又(yòu)稱為(wèi)脂多(duō)糖(lipopolysaccharides,LPS,分(fēn)子量範圍為(wèi)3,000至4,000Da,由長(cháng)鏈複合多(duō)糖尾部和疏水脂質(zhì)基團組成(圖1)),是大多(duō)數格蘭氏陰性菌細胞壁的組成部分(fēn),具(jù)有(yǒu)較高的熱穩定性。當細菌在活躍生長(cháng)或在死亡分(fēn)解時,細胞壁中(zhōng)的脂多(duō)糖就被釋放到周圍環境中(zhōng)。
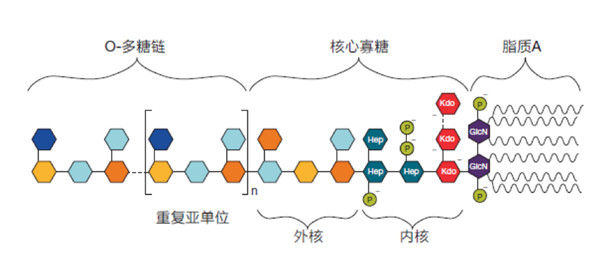
圖1.脂多(duō)糖結構。内毒素為(wèi)複合脂多(duō)糖,是革蘭氏陰性細菌細胞壁的活性結構成分(fēn)。它們由核心寡糖鏈、O-特異性多(duō)糖側鏈(O-抗原)和脂質(zhì)組分(fēn)(脂質(zhì)A)組成。
使用(yòng)如大腸杆菌(E.coli)生産(chǎn)的重組蛋白,或者提取革蘭氏陰性菌内的核酸時經常遇到内毒素污染問題。内毒素污染的蛋白質(zhì)/抗體(tǐ)/核酸在轉染入細胞中(zhōng)或者注入到動物(wù)體(tǐ)内時,可(kě)引發強烈的免疫反應,導緻全身性炎症反應綜合征(SIRS)和/或敗血症。因此,内毒素的去除對于人類疾病治療的注射型藥品、生物(wù)制品等都是必須的,尤其對于基因藥物(wù)、蛋白藥物(wù)、抗體(tǐ)藥物(wù)、疫苗等生物(wù)制品的下遊純化處理(lǐ)來說就顯得非常重要。
中(zhōng)國(guó)藥典的規定
細菌内毒素檢查法(通則 1143)包括兩種方法:凝膠法和光度測定法,後者又(yòu)包括濁度法和顯色法,可(kě)以選用(yòng)其中(zhōng)任何一種方法進行細菌内毒素檢查。凝膠法和光度法各具(jù)優點和局限:
凝膠法
凝膠法的優點是操作(zuò)簡便,供試品在排除幹擾作(zuò)用(yòng)後均可(kě)使用(yòng)凝膠法進行檢驗。
凝膠法的幹擾試驗是确定供試品能(néng)否使用(yòng)凝膠法的決定因素。進行幹擾實驗時,應挑選與鲎試劑反應呈陰性的樣品進行幹擾試驗。若樣品稀釋到 MVD(有(yǒu)效稀釋倍數) 仍不能(néng)排除幹擾作(zuò)用(yòng),應進一步對供試品的前處理(lǐ)進行研究,再用(yòng)幹擾試驗驗證能(néng)否使用(yòng)凝膠法。
光度法
光度法(包括濁度法和顯色法)可(kě)定量檢測内毒素的含量,能(néng)較為(wèi)準确評估産(chǎn)品在生産(chǎn)過程中(zhōng)污染的相對風險,定量檢測的數據不僅有(yǒu)利于追蹤産(chǎn)品質(zhì)量趨勢,還能(néng)起到風險預警的作(zuò)用(yòng),更易達到數據完整性的要求。
由于光度法的檢測限範圍比凝膠法寬,使得有(yǒu)幹擾的樣品可(kě)以有(yǒu)更大的稀釋倍數,對于部分(fēn)使用(yòng)凝膠法無法排除幹擾的樣品,可(kě)以嘗試使用(yòng)光度法建立細菌内毒素檢測方法。
常用(yòng)實驗方法和幹擾分(fēn)析
鲎試劑是從海洋動物(wù)鲎提取的血細胞溶解物(wù),是檢測革蘭氏陰性細菌内毒素的一種敏感試劑。其實驗原理(lǐ)如圖2所示:
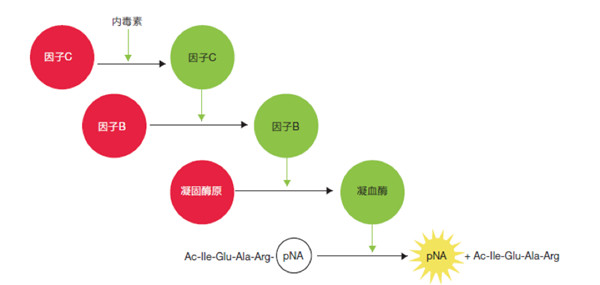
圖2.鲎試劑的級聯反應。LPS(内毒素)激活質(zhì)膜結合因子C。活化的因子C激活因子B,活化的因子B激活凝固酶原,生成凝血酶。加入顯色底物(wù)Ac-Ile-Glu-Ala-Arg-pNA後,活化的蛋白酶-凝血酶催化對硝基苯胺(pNA)的釋放,産(chǎn)生黃色。通過測量405nm處吸光度值進行定量。根據标準曲線(xiàn)可(kě)推算得出結果。紅色表示無活性酶,綠色表示活性酶。
通常實驗流程:
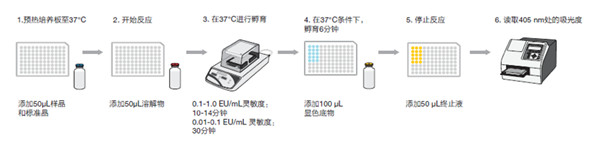
Thermo提供光度法内毒素定量試劑 (A39552)。那麽試劑的品質(zhì)如何?我們将從靈敏度、數據重複性、抗幹擾性等幾個角度對Pierce内毒素定量試劑盒的性能(néng)進行驗證:
數據靈敏度和重複性
提供兩個線(xiàn)性動态範圍:0.01-0.1 EU/mL和0.1-1.0 EU/mL(圖3)。使用(yòng)此試劑盒的實驗-實驗和操作(zuò)者-操作(zuò)者差異系數(CV)為(wèi)3%。靈敏度高可(kě)以有(yǒu)效地避免内毒素定量中(zhōng)潛在的假陰性或者假陽性。
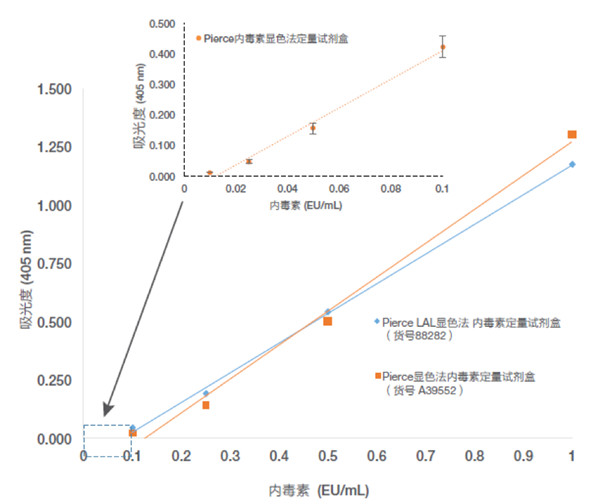
圖3.Pierce内毒素定量試劑盒的标準曲線(xiàn)。标準曲線(xiàn)顯示出優異的線(xiàn)性度,r2= 0.99。Pierce顯色法内毒素定量試劑盒的較低标準曲線(xiàn)範圍為(wèi)0.01-0.1 EU/mL。0.1–1.0 EU/mL标準曲線(xiàn)表示使用(yòng)内毒素标準品和阿米巴樣細胞裂解物(wù)培養14分(fēn)鍾,随後使用(yòng)顯色底物(wù)培養6分(fēn)鍾。對于較低濃度,使用(yòng)内毒素标準品和阿米巴樣細胞裂解物(wù)培養30分(fēn)鍾,随後使用(yòng)顯色底物(wù)培養6分(fēn)鍾。低濃度标準品(0.01-0.1 EU/mL)顯示出了一緻性和再現性(n = 17;CV = 3%)。
兼容性
鲎試劑可(kě)能(néng)受許多(duō)因素影響,造成假陰性或假陽性。包括:
i. 反應溫度、樣品酸堿度、離子強度和金屬離子(如鎂和鈣)
ii. 血清蛋白、核酸、脂肪酸、表面活性劑和螯合劑(如EDTA和肝素)可(kě)引起内毒素分(fēn)子結構的變化
iii. (1-3)-β-D-葡聚糖的非特異性幹擾:鲎試劑會與其反應,造成假陽性結果
表1.使用(yòng)Pierce顯色法内毒素定量試劑盒,獲得有(yǒu)效内毒素檢測結果所兼容的高濃度。所列出的濃度是指樣品中(zhōng)添加0.5 EU内毒素時,未使定量值降低的實際濃度。以比例的形式表示稀釋濃度,其中(zhōng)1:100表示100倍稀釋
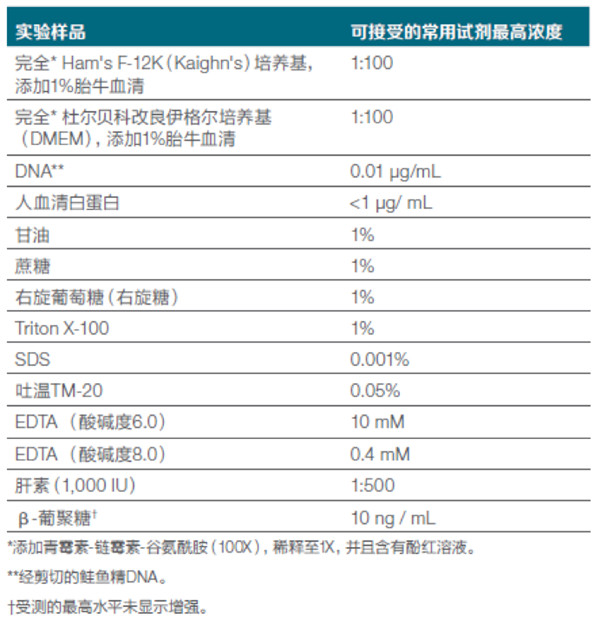
需要指出的是:Pierce顯色法内毒素定量試劑盒(貨号A39552)與β-葡聚糖兼容,并且在含有(yǒu)10ng/ mL(1,3)-β-D-葡聚糖的樣品中(zhōng),未顯示出增強作(zuò)用(yòng)。
内毒素去除
超濾、多(duō)粘菌素B親和樹脂以及基于樹脂或膜的色譜法是内毒素去除的傳統方法,這些方法在蛋白回收率、内毒素結合能(néng)力等方面具(jù)有(yǒu)局限性,有(yǒu)的甚至本身具(jù)有(yǒu)毒。
Thermo Fisher Scientific提供高載量内毒素去除樹脂(88270),是基于ε-聚賴氨酸親和樹脂(天然賴氨酸的聚合物(wù)),顯示出内毒素結合能(néng)力和蛋白質(zhì)回收率:
➤ 結合力可(kě)以達到2,000,000 EU/mL
➤ 在處理(lǐ)初始内毒素水平為(wèi)10,000 EU/mL的樣品時,去除效率可(kě)以達到99%以上
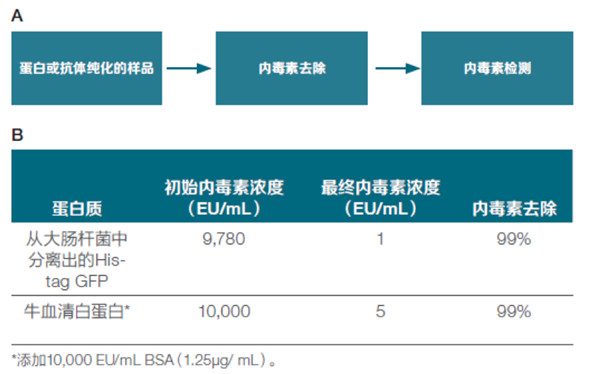
圖4.采用(yòng)Pierce高通量内毒素去除樹脂去除内毒素的效率。(A)内毒素去除和定量的工(gōng)作(zuò)流程。(B)測定和去除蛋白質(zhì)樣品中(zhōng)的内毒素以備下遊應用(yòng)。
