新(xīn)聞中(zhōng)心
不管是在藥物(wù)研發還是基礎科(kē)研中(zhōng),檢測蛋白與小(xiǎo)分(fēn)子的相互作(zuò)用(yòng)都是一類重要的實驗。小(xiǎo)分(fēn)子最主要的特點是分(fēn)子量較小(xiǎo),一般在1000 Da以下;并且結構性質(zhì)各異,部分(fēn)溶解度較差,需要使用(yòng)有(yǒu)機溶劑(例如DMSO等)促溶;這些特點給相互作(zuò)用(yòng)的檢測帶來很(hěn)大的挑戰。基于SPR(表面等離子體(tǐ)共振)原理(lǐ)的Biacore系統具(jù)有(yǒu)靈敏度高、可(kě)進行溶劑校正等優勢,不僅可(kě)以檢測較低的信号,且對分(fēn)子量差異懸殊的互作(zuò)類型也能(néng)精(jīng)确檢測,同時還能(néng)消除有(yǒu)機溶劑帶來的影響,因此越來越多(duō)的研究者選擇Biacore進行蛋白與小(xiǎo)分(fēn)子相互作(zuò)用(yòng)檢測。
我們将根據智荟專線(xiàn)收集到的客戶反饋,針對Biacore系統檢測蛋白與小(xiǎo)分(fēn)子相互作(zuò)用(yòng)實驗中(zhōng)常出現的代表性問題,分(fēn)上下兩篇進行簡單的分(fēn)享與讨論。本篇為(wèi)上篇,将主要圍繞實驗設計和樣品準備方面的問題展開介紹。
一、配體(tǐ)的固定策略以及芯片的選擇
對于配體(tǐ)(固定相)采用(yòng)合理(lǐ)的固定方式并達到所需的固定量,是Biacore實驗邁向成功的第一步。然而所有(yǒu)基于傳感器表面的檢測技(jì )術,都會面臨“物(wù)質(zhì)遷移效應”的影響,所以根據實驗類型及科(kē)學(xué)的偶聯量計算公(gōng)式去控制偶聯量非常關鍵。為(wèi)此,目前僅有(yǒu)Biacore具(jù)備這樣嚴謹的計算公(gōng)式,這其中(zhōng)固定量的計算方式主要就是參考以下核心方程式,并且其不僅适用(yòng)于直接偶聯法的偶聯量計算,也可(kě)用(yòng)于捕獲法的捕獲量計算:

公(gōng)式中(zhōng),RL為(wèi)配體(tǐ)的固定量,Rmax為(wèi)芯片表面的最大結合容量,Sm為(wèi)化學(xué)計量比(未知情況時可(kě)先設為(wèi)1)。此公(gōng)式可(kě)以簡單理(lǐ)解為(wèi),Biacore中(zhōng)産(chǎn)生的響應值信号反映的是芯片表面質(zhì)量的變化。一般情況下,對于動力學(xué)分(fēn)析,要求Rmax ≤ 50 RU;對于親和力分(fēn)析,要求Rmax ≤ 100 RU。由此計算得到理(lǐ)論固定量RL,在偶聯法中(zhōng)實際固定量可(kě)能(néng)需要1.5~3RL;在捕獲法中(zhōng),則可(kě)以按照理(lǐ)論固定量來設定配體(tǐ)的捕獲量,因為(wèi)捕獲過程的分(fēn)子朝向固定,條件一般也是溫和的接近中(zhōng)性,最大程度地保留的配體(tǐ)分(fēn)子的活性。
對于上面的核心方程式有(yǒu)了基本的了解之後,就可(kě)以回答(dá)下面這些問題了。
1是選擇固定蛋白還是固定小(xiǎo)分(fēn)子?
首先需要明确的是,如果您的實驗目的是想獲得精(jīng)确的親和力數值,那建議選擇固定蛋白。考慮到小(xiǎo)分(fēn)子的固定難度、空間位阻以及固定過程對于結合的影響等方面的問題,選擇氨基偶聯的方式固定蛋白往往是最簡單、有(yǒu)效的固定方式。而小(xiǎo)分(fēn)子本身的活性基團有(yǒu)限,基團的反應活性也與蛋白存在一定的差異,偶聯條件需要摸索,另外,通過這些基團的偶聯反應可(kě)能(néng)也破壞了小(xiǎo)分(fēn)子僅有(yǒu)的結合反應活性位點。因此,隻有(yǒu)對于某些特定類型的定性實驗,比如分(fēn)子垂釣,固定小(xiǎo)分(fēn)子也是可(kě)行的,通常推薦的固定方式是使用(yòng)SA芯片固定生物(wù)素修飾後的小(xiǎo)分(fēn)子,可(kě)以在比較明确的條件下實現穩定的固定,而且生物(wù)素分(fēn)子在一定程度上可(kě)以起到間隔臂(spacer arm)的作(zuò)用(yòng),減少小(xiǎo)分(fēn)子結合受到的空間位阻影響。
綜上所述,固定蛋白的過程相對簡單也适用(yòng)于大多(duō)數結合反應,因此是目前探究蛋白與小(xiǎo)分(fēn)子互作(zuò)時最常用(yòng)的選擇。
2固定蛋白是選擇直接偶聯還是捕獲法?
先說結論:我們建議,進行蛋白與小(xiǎo)分(fēn)子互作(zuò)實驗時優先考慮直接偶聯蛋白的方式。
直接偶聯(氨基偶聯)法的操作(zuò)方法較簡便、明确,而且可(kě)以實現較高的偶聯量,在小(xiǎo)分(fēn)子作(zuò)為(wèi)分(fēn)析物(wù)時,有(yǒu)利于獲得比較理(lǐ)想的響應值。例如常用(yòng)的CM5芯片,最高偶聯量可(kě)以到10000 – 15000 RU,非常适合蛋白與小(xiǎo)分(fēn)子此類分(fēn)子量差異懸殊的檢測。除了直接偶聯法以外,根據樣品性質(zhì)與分(fēn)子量差異,捕獲法也是一種您可(kě)以選擇的固定策略,例如:待固定的樣品未經純化,含有(yǒu)其他(tā)雜質(zhì);或者擔心直接偶聯的過程會影響結合位點等。在這些情況下,可(kě)以考慮通過捕獲法固定配體(tǐ)。當配體(tǐ)樣品的純度不夠時,捕獲的過程相當于在芯片表面進行了一次在線(xiàn)純化;捕獲過程的條件較為(wèi)溫和,可(kě)以盡可(kě)能(néng)地保留配體(tǐ)的結合活性,同時保證配體(tǐ)自由朝向,充分(fēn)暴露結合位點。
常用(yòng)的捕獲類芯片以NTA芯片為(wèi)例,這是一種可(kě)以通過螯合鎳離子捕獲帶有(yǒu)His标簽蛋白的捕獲芯片。如下圖1所示,NTA芯片上捕獲量大約在3000 – 4000 RU[1]最為(wèi)穩定,非常适合His标簽蛋白與小(xiǎo)分(fēn)子二者分(fēn)子量差異不是特别大的親和力檢測。

1. 在NTA芯片上,不同捕獲量水平下基線(xiàn)的穩定情況[1]。
3氨基偶聯蛋白配體(tǐ)是選擇CM5芯片還是CM7芯片?
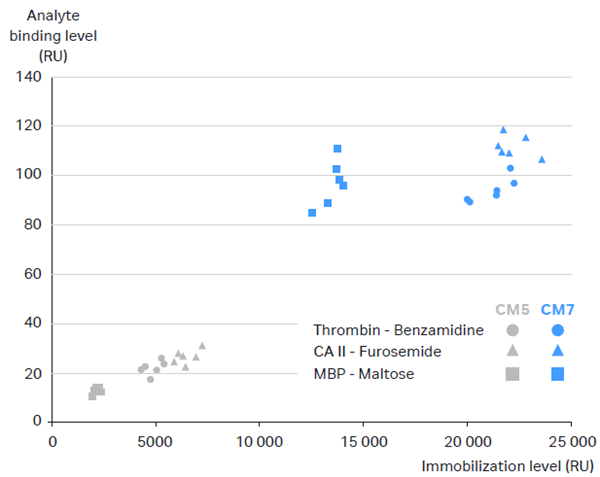
CM5與CM7芯片表面均為(wèi)羧甲基化修飾的葡聚糖基質(zhì),兩者最主要的區(qū)别是CM7芯片的羧基含量顯著高于CM5芯片,因此可(kě)以實現更高的偶聯量。圖2比較了三對蛋白與小(xiǎo)分(fēn)子的互作(zuò)在CM5和CM7芯片上的結果差異,可(kě)以看到同一組互作(zuò)實驗,在CM7芯片上可(kě)以達到的偶聯量和分(fēn)析物(wù)響應值為(wèi)CM5芯片的3倍以上 [2] 。
2. 三組蛋白與小(xiǎo)分(fēn)子互作(zuò)在CM5和CM7芯片上的偶聯量與分(fēn)析物(wù)響應值比較[2]。
如上所述,CM5芯片的最高偶聯量在10000 – 15000 RU左右,如果按照固定量計算公(gōng)式得到的理(lǐ)論偶聯量遠(yuǎn)超這個範圍,則可(kě)以考慮使用(yòng)CM7芯片。簡單來說,當蛋白與小(xiǎo)分(fēn)子的分(fēn)子量比值大于100時,就建議考慮換用(yòng)CM7芯片。
二、樣品準備的相關問題
在确定了配體(tǐ)的固定策略,并選定了相應的芯片之後,就可(kě)以開始下一步的實驗了。進入試劑、樣品的準備階段,又(yòu)會遇到哪些問題呢(ne)?我們接着往下看。
如何選擇運行緩沖液?
目前Cytiva供應的用(yòng)于Biacore實驗的運行緩沖液主要有(yǒu)兩大類,分(fēn)别是基于HEPES緩沖體(tǐ)系的HBS系列緩沖液與基于磷酸鹽緩沖體(tǐ)系的PBS系列緩沖液。
在選擇運行緩沖液時,并沒有(yǒu)明确的規定必須使用(yòng)何種緩沖液,應該根據分(fēn)子互作(zuò)的自身性質(zhì)選擇合适的緩沖液。一般來說,有(yǒu)以下經驗可(kě)供參考:當分(fēn)析物(wù)是小(xiǎo)分(fēn)子的情況下可(kě)以首先嘗試PBS 或者PBS-P+緩沖液;而分(fēn)析物(wù)為(wèi)蛋白時可(kě)以首先嘗試HBS或者HBS-EP+緩沖液。
在一些情況下,小(xiǎo)分(fēn)子的溶解需要一定濃度的有(yǒu)機溶劑助溶,例如5% DMSO等,而這些有(yǒu)機溶劑在不同樣品之間的濃度差異會幹擾響應值信号,因此需要對這部分(fēn)由運行緩沖液造成的信号進行校正——溶劑校正。而有(yǒu)機溶劑自動校正的功能(néng),也是Biacore的絕活兒之一,充分(fēn)保證了最終實驗結果真實可(kě)信。關于溶劑校正的相關問題将在下篇中(zhōng)進行讨論。
需要準備多(duō)少的蛋白用(yòng)來偶聯?
實驗準備的配體(tǐ)蛋白量,至少要足夠其達到所需的偶聯量。下表展示了要達到不同的偶聯水平時所需的配體(tǐ)濃度以及相應的配體(tǐ)偶聯時間(流速為(wèi)10 μL/min),可(kě)供參考[3]。需要注意的是,表中(zhōng)列出的“配體(tǐ)工(gōng)作(zuò)濃度”是用(yòng)偶聯緩沖液醋酸鈉稀釋配體(tǐ)蛋白樣品後的濃度。為(wèi)了讓稀釋後的蛋白樣品能(néng)夠充分(fēn)富集在芯片表面,醋酸鈉的稀釋倍數一般要在20倍以上;如果稀釋倍數不夠,将影響配體(tǐ)蛋白偶聯效率。因此,準備配體(tǐ)蛋白母液時最好在工(gōng)作(zuò)濃度的20倍以上。
表1. 偶聯量與配體(tǐ)工(gōng)作(zuò)濃度參考表[3]。
對于一個未知的實驗,摸索合适的偶聯量等過程是必不可(kě)少的,因此對于蛋白配體(tǐ)的用(yòng)量也不應僅限于夠一次偶聯實驗使用(yòng)。一般的建議是,配體(tǐ)蛋白的準備量在1 mg/mL濃度、50 μL以上。但即便如此,老師們也能(néng)清晰的算出來Biacore對于蛋白的用(yòng)量非常低,遠(yuǎn)遠(yuǎn)優于您其他(tā)的互作(zuò)檢測手段。
小(xiǎo)分(fēn)子分(fēn)析物(wù)的濃度範圍如何确定?
不管在動力學(xué)(Kinetics)分(fēn)析還是在親和力(Affinity)分(fēn)析中(zhōng),分(fēn)析物(wù)濃度範圍的确定均與結合反應的解離平衡常數(KD)有(yǒu)關。一般設置的分(fēn)析物(wù)濃度梯度範圍如果能(néng)夠覆蓋KD值,将會達到較準确的拟合結果。在動力學(xué)分(fēn)析中(zhōng),一個理(lǐ)想的分(fēn)析物(wù)濃度範圍可(kě)以從10 × KD作(zuò)為(wèi)最高濃度進行梯度稀釋;在親和力分(fēn)析中(zhōng),理(lǐ)想的分(fēn)析物(wù)濃度範圍可(kě)以選擇從2 × KD的濃度作(zuò)為(wèi)最高濃度進行梯度稀釋[4]。對于蛋白與小(xiǎo)分(fēn)子的互作(zuò),大多(duō)數情況下是“快結合快解離”的模式,适用(yòng)于親和力分(fēn)析的模型(關于數據分(fēn)析中(zhōng)模型選擇的問題,将會在下篇中(zhōng)進行讨論)。蛋白與小(xiǎo)分(fēn)子結合反應的KD值,基本都在μM級别,因此可(kě)以将小(xiǎo)分(fēn)子最高濃度設為(wèi)1000 μM,按照3倍甚至5倍的稀釋比例來配制濃度梯度(拉大範圍)。進行這樣的初步實驗後,基本可(kě)以确定反應KD值的大緻範圍,後續可(kě)以調整濃度範圍、減小(xiǎo)稀釋比例再進行進一步實驗。當然,小(xiǎo)分(fēn)子能(néng)夠達到的最高濃度還受到溶解度等因素的影響。
以上是針對Biacore檢測蛋白與小(xiǎo)分(fēn)子互作(zuò)的實驗方案設計以及樣品準備方面的常見問題分(fēn)享。良好的開端是成功的一半,合理(lǐ)的活性配體(tǐ)偶聯量、分(fēn)析物(wù)濃度範圍以及運行緩沖液選擇,将幫助我們得到更理(lǐ)想的實驗結果。在下篇中(zhōng)我們将繼續分(fēn)享關于實驗進行以及數據分(fēn)析方面的常見問題,敬請期待!
文(wén)章來源:https://mp.weixin.qq.com/s/sG_kZkA5Kcdory0KPagPgw
